|
2011/1
No.111 |
1. 巻頭言 | 2. ICA 2010 | 3. IWRN10に参加して | 4. カンカン石(サヌカイト) | |||||||
|
|
5. 医薬業界向けパーティクルカウンタKL-04A | ||||||||||
<技術報告>
![]() 医薬業界向けパーティクルカウンタKL-04A
医薬業界向けパーティクルカウンタKL-04A
リオン株式会社 環境機器事業部 開発部 今 井 雄 大
 図1 KL-04Aの外観 |
|
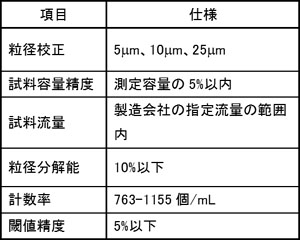
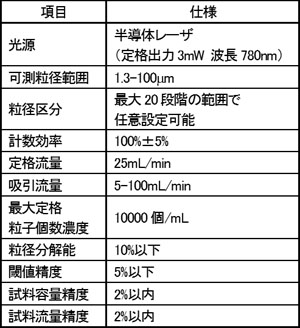
表1 KL-04Aの主な仕様
 |
|
|
1. はじめに
弊社の微粒子計は、半導体デバイス業界を始めとして、様々な分野で使用されている。医薬業界もその活躍している分野の一つである。 点滴等の注射剤は直接人体に注入されるため、異物の混入は最悪の場合、患者に影響を及ぼすことがある。このため、薬品の製造工程や品質管理には異物混入に関して厳重な管理が求められる。日本薬局方(The
Japanese Pharmacopeia; JP)には注射剤中の不溶性微粒子の個数濃度が定められているが、試験を行なう微粒子計についても、その性能に対する試験項目が定められている。また、薬局方の他にも医薬業界においては遵守すべき規制が存在する。これは外国においても同様である。
弊社の従来製品KL-04は、これらの規制および試験に対応する機能を持つ製品として高い評価を得てきた。このたび、KL-04に機能を追加した光遮蔽型自動微粒子計測装置KL-04Aを開発した。医薬品の品質管理には複雑な規制が求められるので、これらの簡単な解説と併せて製品の特徴を紹介する。図1にKL-04Aの外観図を示す。
2. 製品の特徴
KL-04Aの主な仕様を表1に示す。本製品の特徴は以下の通りである。
(1) 一体型
本製品は試料設置台、センサ、シリンジサンプラ、信号処理部、画面表示部が一体となっている。他社製品ではこれらが分離しているものもある。一体型であるメリットとして、単体で測定可能である、持ち運びが容易である、測定系による誤差要因が少ない、等が挙げられる。また、試料設置台にはスターラを搭載することができ、試料の攪拌が可能である。
図2はKL-04Aの測定画面である。パラメータの入力や機器の各種設定はキーボードやマウスを操作して行う。測定開始/停止の制御はマウスでも可能だが、本体のボタンを押すことでも可能である。
(2) 各国薬局方の試験機能
JPの「6.07 注射剤の不溶性微粒子試験法」にて、注射剤中に許容される微粒子の個数と、その測定に使用される微粒子計が満たすべき性能試験項目が記載されている。米国薬局方(The
United States Pharmacopeia; USP)、欧州薬局方(The European Pharmacopeia; EP)、大韓薬典(The
Korean Pharmacopeia; KP)にも相当の試験法が定められている。その内容を表2に示す。また、JPにおいて装置の満たすべき試験項目を表3に示す。
KL-04Aはこれらの試験のうち、試料容量、試料流量を除く試験を行なうことができる。また、測定結果が図2に示す規格を満たすことの合否を判定できる。試験条件の設定は自由に行うことができ、複数パターンの条件を保存しておくことができる。行った粒径校正、性能試験、測定結果、およびこれらの試験条件は全て内蔵のHDDに保存される。
これらの性能試験については、工場出荷時オプションとして、弊社でも行っている。
|
表2 各国薬局方における不溶性微粒子試験の判定規格
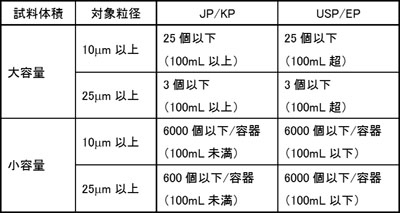 |
表3 JP 「6.07 注射剤の不溶性微粒子試験法」における装置試験の規格 |
(3) 電子記録、署名への対応
アメリカFDA (Food and Drug Administration; 食品医薬品局)の規制である「Title 21 Code of Federal
Regulations Part 11: Electronic Records; Electronic Signatures; 21 CFR Part
11」では、記録改ざんのような不正を排除するため、計測器による測定結果の完全性の証明と、ファイルの変更や操作に関する履歴の自動記録(オーディットトレイル)についても求めている。
KL-04Aは21 CFR Part 11を初めとした電子記録、電子署名に関する規制対応の機能を有している。HDDに作成されたファイルには個別に指紋が作成され、KL-04Aはこれを調べることでファイルの改ざんを検知する。また、HDDに保存されたデータをUSBメモリによってバックアップ・リストアすることが可能である。測定データの作成、変更、削除など、電子記録に関する主要な動作をオーディットトレイルとして記録し、その閲覧、印刷ができる。ただし、署名機能については、手書き署名の対応となる。
(4) ユーザごとの権限設定
21 CFR Part 11ではシステム設定へのアクセス制限やデータのセキュリティについても定めている。 管理権限を持つユーザは、ユーザ毎に測定データの変更・削除、システム設定の変更に関するアクセス権限を設定することが可能であり、高いセキュリティ性を実現している。
(5) シリアル通信によるコンピュータへのデータ出力
USB-RS-232C 変換ケーブル(別売品)を接続することで、測定ごとにシリアル通信によるコンピュータへのデータ出力が可能である。KL-04Aでの新機能である。
(6) USBメモリによるデータ出力
USB メモリを用いて、HDDに保存されている測定データを TSV(Tab Separated Values)形式で取り出すことができる。
(7) プリンタによる出力
プリンタを接続することにより、測定結果等を印刷することができる。対象プリンタはPostScript Level 2 以降をサポートしているものである。
(8) 外部ディスプレイへの出力
KL-04Aの内蔵LCDは6.5インチであるが、市販のPC用ディスプレイを接続することで、大きなデスクトップ領域が拡大する。これにより作業性が向上する。
3. バリデーション業務のサポート
バリデーションとは、試験条件や作業プロセスなどが適切であるか科学的に検証して文書化し、この方法にて装置が期待される結果を得ていることを記録として文書化、保存することである。この作業も医薬業界で薬事法に基づき求められるものであるが、書類作成にかかる作業量が膨大かつ煩雑であるため、弊社にて業務のサポートを行っている。
弊社でサポートする業務を以下に示す。
(1) 設備据付時適格性評価(IQ)
IQ(Installation Qualification)は製品の据付時に正しく据え付けられていることの確認である。納入品目の確認、納入製品の外観確認、製品の初期状態の確認、これら確認事項の記録の作成を行う。
(2) 運転時適格性評価(OQ)
OQ(Operation Qualification)は、製品が仕様通りの機能、性能が得られていることの確認である。操作状況の確認、製品の各機能が仕様などを満足していることの確認、これら確認事項の記録の作成を行う。
(3) 性能的確性評価(PQ)
PQ(Performance Qualification)は、製品が実際の稼動時において必要な性能を満たしていることの確認である。KL-04Aの場合には、各薬局方に定められた性能試験を行なう。
(4) 標準作業手順書(SOP)
SOP(Standard Operation Procedure)は、測定や試験の手順、必要な器材の詳細を定めた書類である。KL-04Aでは、ユーザがPQ作業として、定期的に装置の性能確認を行うためのSOPを提供する。
4. 終わりに
弊社の医薬業界向け微粒子計であるKL-04Aを紹介した。前器種のKL-04は複雑な規制要件に対して充実した機能にて対応を行ってきた。KL-04Aにおいても引き続きお客様の品質管理に役立つことができれば幸いである。